Selon un groupe de chercheurs de l'Université de Pennsylvanie, la puissance du soleil, du vent et de la mer pourrait bientôt s'unir pour produire de l'hydrogène, un carburant respectueux de l'environnement. L'équipe a intégré la technologie de purification de l'eau dans un nouveau projet expérimental électrolyseur d'eau de mer, qui utilise un courant électrique pour séparer l'hydrogène et l'oxygène dans les molécules d'eau.
Selon Bruce Logan, professeur d'ingénierie environnementale à Kappa et professeur à l'université Evan Pugh, cette nouvelle méthode de "division de l'eau de mer" pourrait faciliter la conversion de l'énergie éolienne et solaire en carburants stockables et portables.
"L'hydrogène est un excellent carburant, mais vous devez l'obtenir", a déclaré Logan. - La seule façon durable d'y parvenir est d'utiliser des énergies renouvelables et de les produire à partir de l'eau. Il faut aussi utiliser de l'eau que les gens ne veulent pas utiliser à d'autres fins, c'est-à-dire de l'eau de mer. Ainsi, le Saint Graal de la production d'hydrogène devait combiner l'eau de mer, l'énergie éolienne et solaire trouvée dans les environnements côtiers et marins."
Malgré l'abondance de l'eau de mer, elle n'est généralement pas utilisée pour la séparation de l'eau. Si l'eau n'est pas dessalée avant d'être introduite dans l'électrolyseur – une étape supplémentaire coûteuse – les ions chlore de l'eau de mer se transforment en chlore gazeux toxique, qui détruit l'équipement et s'infiltre dans l'environnement.
Pour éviter cela, les chercheurs ont inséré une fine membrane semi-perméable conçue à l'origine pour purifier l'eau lors d'un traitement par osmose inverse (OI). La membrane d'osmose inverse a remplacé la membrane échangeuse d'ions couramment utilisée dans les électrolyseurs.
"L'idée derrière l'osmose inverse est que vous mettez une pression très élevée sur l'eau, la poussant à travers la membrane et gardant les ions chlore derrière", a déclaré Logan.
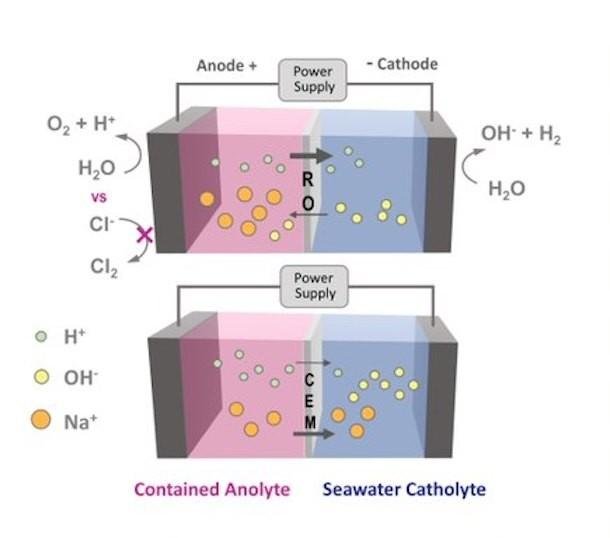
Dans l'électrolyseur, l'eau de mer ne traversera plus la membrane d'osmose inverse, mais sera retenue par celle-ci. La membrane est utilisée pour séparer les réactions se produisant à proximité de deux électrodes immergées - une anode chargée positivement et une cathode chargée négativement - connectées à une source d'alimentation externe. Lorsque le courant est allumé, les molécules d'eau commencent à se diviser à l'anode, libérant de minuscules ions d'hydrogène appelés protons et formant de l'oxygène gazeux. Les protons traversent ensuite la membrane et se combinent avec les électrons à la cathode pour former de l'hydrogène gazeux.
Avec une membrane d'osmose inverse installée, l'eau de mer reste du côté de la cathode et les ions chlore sont trop gros pour traverser la membrane et atteindre l'anode, empêchant la formation de chlore gazeux.
Mais dans la séparation de l'eau, comme l'a souligné Logan, d'autres sels sont délibérément dissous dans l'eau pour la rendre conductrice. La membrane échangeuse d'ions, qui filtre les ions par charge électrique, laisse passer les ions de sel. Il n'y a pas de membrane d'osmose inverse.
Étant donné que le mouvement des ions plus gros est limité par la membrane RO, les chercheurs devaient tester si les minuscules protons se déplaçant à travers les pores étaient suffisants pour maintenir un courant électrique élevé.
Dans une série d'expériences, les chercheurs ont testé deux membranes d'osmose inverse disponibles dans le commerce et deux membranes échangeuses de cations, un type de membrane échangeuse d'ions qui permet le mouvement de tous les ions chargés positivement dans le système. Chacun d'eux a été testé pour la résistance de la membrane au mouvement des ions. La quantité d'énergie nécessaire pour achever les réactions a également été calculée, la formation d'hydrogène et d'oxygène gazeux a été surveillée, l'interaction avec les ions chlore et les dommages à la membrane ont été analysés.
Les chercheurs ont récemment reçu une subvention de 300 000 $ de la National Science Foundation (NSF) pour poursuivre leurs recherches sur l'électrolyse de l'eau de mer. Logan espère que leurs recherches joueront un rôle crucial dans la réduction des émissions de dioxyde de carbone dans le monde.
Lisez aussi:
- TSMC : en 2021, des copies de test des processeurs 3nm feront leur apparition
- La gravité cause l'uniformité de l'univers
